免疫检查点抑制剂(Immune checkpoint inhibitors, ICIs)越来越多地用于晚期肝细胞癌(Hepatocellular carcinom, HCC)患者。目前评估ICIs治疗的临床试验大多数针对的是肝功能Child-Pugh A级患者,然而临床实践中许多晚期HCC患者的肝功能为Child-Pugh B级,这导致在临床上对合并有肝功能受损的晚期HCC患者使用ICIs治疗的相关证据缺乏。
针对上述问题,西安交通大学第二附属医院感染科纪泛扑教授团队、洛杉矶Cedars-Sinai Medical Center杨毅辉和Ju Dong Yang博士团队、伦敦Imperial College London,David J. Pinato教授团队合作开展研究。该研究通过荟萃分析22项已发表研究,总共纳入699名Child-Pugh B级和2114名Child-Pgh A级的晚期肝细胞癌患者,系统分析了ICIs治疗Child-Pugh B级肝功能晚期肝细胞癌患者的疗效和耐受性。研究同时获得包括美国、日本、德国、奥地利、中国河北、台湾地区团队7项研究原始数据资料的数据支持与协作。
研究发现接受ICIs治疗的Child-Pugh B级晚期肝细胞癌患者的客观应答率(objective response rate,ORR)为14%(95%CI,11%-17%)(图1A),疾病控制率(disease control rate, DCR)为46%(95%CI,36%-56%)(图1B);其中位生存期为5.5个月(95%CI,3.57-7.42),中位无进展生存期为2.7个月(95%CI,1.85-3.52)。在接受ICIs治疗的晚期肝细胞癌患者中,与Child-Pugh A级相比,Child-Pugh B级的ORR(OR 0.59;95%CI 0.43-0.81;P<0.01)(图1C)和DCR(OR 0.64;95%CI,0.50-0.81;P<0.01)较低(图1D)。Child-Pugh B级肝功能与患者的总生存期短独立相关(未调整的hazard ratio(HR), 2.72 [95%CI,2.34-3.16];调整后的HR为2.33[95%CI,1.81-2.99]。此外,Child-Pugh B级肝功能也与较差的无进展生存期相关,HR为1.69(95%CI 1.41-2.03)。在治疗耐受性方面,Child-Pugh B级患者中任何级别治疗相关不良事件(treatment-related adverse events , trAEs)发生率为40%(95%CI 34%-47%),≥3级trAE发生率为12%(95%CI 6%-23%);任何级别的免疫治疗相关不良事件发生率(immunotherapy-related adverse event,irAE)为31%(95%CI,19%-46%);≥3级的irAE发生率为7%(95%CI 4%-13%)。重要的是,与Child-Pugh A级相比,Child-Pugh B级的任何级别trAE或≥3级trAE的发生率没有增加(表1)。
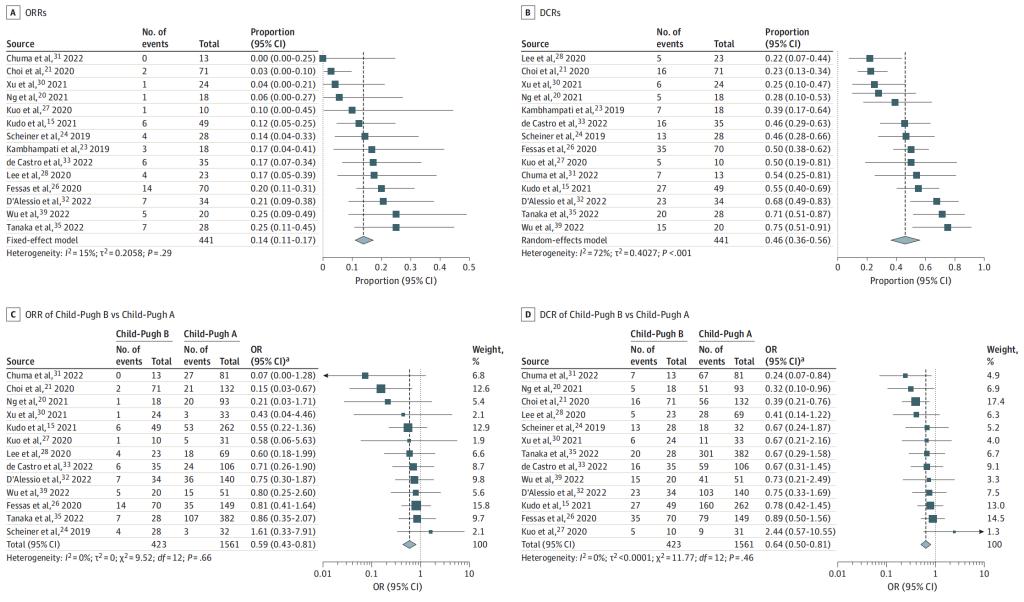
图1.使用ICIs治疗合并Child-Pugh B级肝功能晚期HCC患者的疗效分析
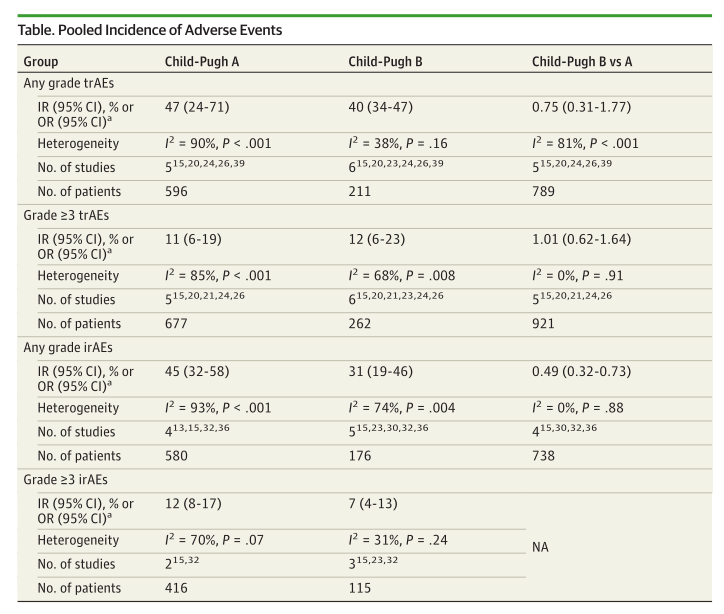
表1.ICIs治疗Child-Pugh B级肝功能的晚期肝细胞癌患者的安全性分析
Child-Pugh B级晚期肝细胞癌患者的治疗问题在临床上备受关注,通过该研究表明Child-Pugh B级晚期肝细胞癌患者使用ICIs治疗尽管总体疗效低于Child-Pugh A级的患者,但有相当一部分患者获得肿瘤应答,且安全性与Child-Pugh A级患者无差别,研究数据支持在精心选择的晚期肝细胞癌和Child-Pugh B级肝功能患者中使用免疫疗法。总体而言该研究为免疫治疗在晚期肝细胞癌患者的应用中提供了更充实的证据支持,但未来仍需要更多的研究来确定ICIs治疗在这一人群中的有效性。
上述研究成果以“Immune Checkpoint Inhibitors for Child-Pugh Class B Advanced Hepatocellular Carcinoma: A Systematic Review and Meta-Analysis”为题在美国医学会肿瘤学期刊《JAMA Oncology》发表交大二附院为第一作者和通讯作者单位,内科学传染病专业博士生谢恩睿为第一作者,杨毅辉博士和Bernhard Scheiner博士为共同第一作者;感染科纪泛扑为末位通讯作者,Ju Dong Yang教授和David J. Pinato教授为共同通讯作者。
论文链接:https://jamanetwork.com/journals/jamaoncology/fullarticle/2808728