放射治疗是肿瘤治疗领域重要的治疗手段,其通过直接造成肿瘤细胞DNA断裂杀死肿瘤细胞,或间接通过激活免疫反应介导远隔效应抑制肿瘤[1]。与此同时,放射治疗可介导促肿瘤免疫反应,削弱疗效甚至导致治疗失败,这提示放射治疗引起的免疫反应具有两面性[2-4]。研究放射治疗引起“双向”作用的免疫学机制,探究如何科学制定放射-免疫联合治疗策略,可为肿瘤多学科综合治疗提出新的方向。
2026年3月19日,第一附属医院肿瘤放疗科韩苏夏/马瑾璐团队及基础医学院侯玉柱团队完成重要研究成果《CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response》(CXCR5+单核细胞向外迁移抑制放射治疗介导的抗肿瘤免疫应答),在Nature Communications发表。该研究首次发现CXCR5+单核细胞在放射抵抗中的重要作用,CXCR5+单核细胞的产生、迁移、功能,以及分化几个方面阐明了其抑制放射治疗介导的抗肿瘤免疫反应的机制,为放射-免疫联合治疗提供了理论依据,为肿瘤的综合治疗提供了新的治疗策略。

研究发现单核细胞富集于受照后的肿瘤组织,其中CXCR5+单核细胞显著增加;小鼠荷瘤后,其外周血和骨髓中CXCR5+单核细胞数量和比例升高,提示骨髓和外周血充当CXCR5+单核细胞的“储备池”。进一步研究发现:肿瘤来源的VEGF可通过激活PI3K/Akt/mTOR/HIF1-α通路,诱导骨髓中的单核细胞表达CXCR5。射线促进肿瘤细胞产生趋化因子CXCL13,其作为CXCR5的特异性配体,促使CXCR5+单核细胞由“储备池”浸润至照射后的肿瘤组织。CXCR5+单核细胞高表达PD-L1,通过PD-1/PD-L1轴抑制CD8+ T细胞,使CTL数量减少、功能下降,抑制放射治疗的效果。同时,照射后的肿瘤组织GM-CSF蛋白水平升高,其诱导CXCR5+单核细胞向CXCR5+ M2样的巨噬细胞分化,这群细胞同样发挥着抑制CD8+ T细胞的功能。
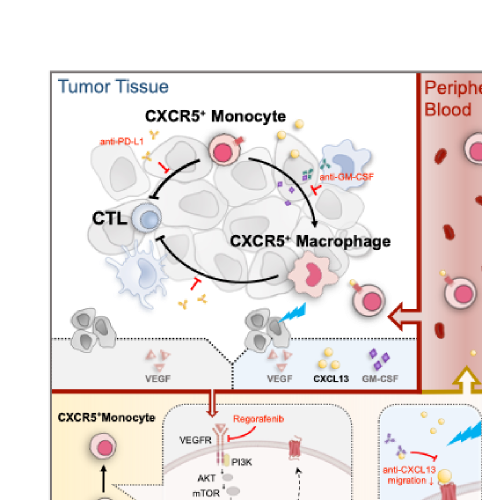
研究团队检测患者放射治疗前后肿瘤组织及外周血的单核细胞,结果表明受照肿瘤中存在CXCR5+单核细胞浸润,且放射治疗后进展的患者外周血单核细胞比例显著升高。在放射治疗时联合阻断CXCR5-CXCL13轴、抑制PD-1/PD-L1信号,中和GM-CSF,最终有效提升放射治疗的效果。阐明其机制为完善综合治疗策略,改善肿瘤患者预后提供了新的方向。
1.Wang, L., et al., Radiotherapy and immunology. J Exp Med, 2024. 221(7).
2.Piffko, A., et al., Radiation-induced amphiregulin drives tumour metastasis. Nature, 2025. 643(8072): p. 810-819.
3.Wang, L., et al., YTHDF2 inhibition potentiates radiotherapy antitumor efficacy. Cancer Cell, 2023. 41(7): p. 1294-1308 e8.
4.Hou, Y., et al., Radiotherapy Enhances Metastasis Through Immune Suppression by Inducing PD-L1 and MDSC in Distal Sites. Clin Cancer Res, 2024. 30(9): p. 1945-1958.
原文链接:https://www.nature.com/articles/s41467-026-70858-6