DNA双链断裂(double-strand break, DSB)是细胞面临的最为致命的DNA损伤形式。为维持基因组稳定性,细胞必须对DSB进行快速而有效的修复。在哺乳动物细胞中,非同源末端连接(non-homologous end joining, NHEJ)是修复DSB的主要途径。其中,DNA末端联会,即将两条断裂的DNA末端在三维空间中拉近并对齐,是NHEJ修复过程中最为关键的步骤。目前针对平末端DNA的NHEJ联会机制已有深入的研究,但由于DNA损伤形式多样,细胞内广泛存在具有不同构型甚至携带碱基损伤的DNA断裂末端,这些末端如何影响联会过程及修复结果仍缺乏系统解析。
近日,西安交通大学基础医学院赵柏林教授研究团队在Nature Communications杂志上发表了题为“DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging”的研究论文。该研究在单分子水平上系统阐明了DNA断裂末端构型在调控NHEJ介导的DNA末端联会过程中的关键作用(图1),并揭示了其对NHEJ修复效率与保真度的重要影响。
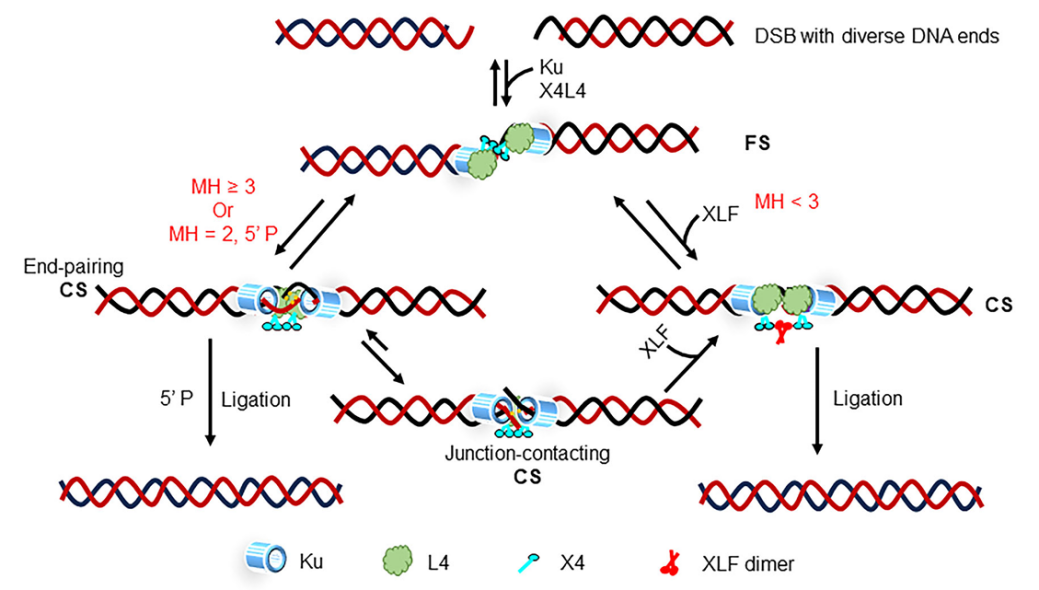
图1:DNA断裂末端构型决定NHEJ修复过程中DNA末端联会通路选择的机制模型。
研究团队前期工作发现,NHEJ核心修复因子Ku70–Ku80、XRCC4–LIG4和XLF可介导平末端DNA形成两种结构不同的联会复合物:可变联会复合物(flexible synaptic complex, FS)和紧密接触联会复合物(close synaptic complex, CS),其中XLF是CS复合物形成所必需的关键因子。只有当DNA断裂末端处于CS复合物中时才可被修复蛋白复合物XRCC4-LIG4连接,完成DSB的修复。
在本研究中,研究团队依托实验室自主搭建的单分子荧光成像平台,结合单分子荧光共振能量转移(single-molecule FRET, smFRET)技术,进一步揭示了DNA断裂末端构型在NHEJ联会通路选择中的决定性作用。研究发现,在缺失XLF的条件下,Ku70–Ku80和XRCC4–LIG4仍可直接介导带有3个核苷酸微同源序列的DNA断裂末端形成CS复合物,表明末端间的微同源碱基配对可在一定程度上补偿XLF功能缺失,确保修复过程的顺利进行。进一步研究表明,XLF能够显著稳定并促进CS复合物的形成,并且含有碱基损伤(如8-oxo-G)的DNA断裂末端并不会影响该联会机制。
此外,研究团队对CS复合物中DNA末端的空间构象进行了深入解析,发现在初始形成的CS复合物中,两条DNA末端的单链–双链交界区域紧密相邻,而单链部分则垂悬向外延伸。这种特殊的空间排列有利于断裂末端微同源序列的搜索,并为NHEJ修复过程中相关核酸酶和聚合酶对不兼容末端的加工处理提供了结构基础。该研究系统拓展了NHEJ介导的DNA末端联会机制,揭示了其在应对多样化DNA损伤时所表现出的结构与功能多样性,为理解NHEJ通路如何高效修复DSB提供了新的分子层面认识。
本研究以西安交通大学基础医学院为第一完成单位。基础医学院刘迪助理教授和赵柏林教授为论文共同通讯作者,基础医学院博士研究生张晨阳为论文共同第一作者(第一位)。深圳湾实验室尹延东研究员对本研究给予了重要支持。该研究得到国家自然科学基金、中国博士后科学基金、陕西省“三秦英才”引进计划、西安交通大学青年拔尖人才支持计划及基本科研业务费等项目的资助。
论文链接:https://doi.org/10.1038/s41467-026-68417-0