6月6日,西安交大一附院精神心理科马现仓、高媛团队在精神领域权威期刊《大脑、行为和免疫》(Brain Behavior and Immunity)(中科院1区)上发表原创研究论文《Nod2 deficiency exacerbates schizophrenia-related alterations in offspring of maternal immune activation in a sex-dependent manner》(《Nod2缺失以性别特异性方式加剧母体免疫激活后代的精神分裂症相关改变》),该研究首次建立了Nod2缺失和母体免疫激活的双打击模型,进一步揭示了肠道菌群-免疫-脑轴在精神分裂症发生发展中的关键作用机制。

精神分裂症是一种严重的精神障碍,全球患病率约为1%,是世界十大主要致残原因之一。既往很多研究揭示了遗传、环境、肠道菌群等因素是导致精神分裂症发生的关键原因,然而其具体的分子机制仍不清楚。马现仓教授团队前期研究发现精神分裂症的发生与肠道微生物紊乱有关,肠道生态失调导致肠道衍生细菌产物向体循环的转运增加,促进炎症和其他与精神分裂症有关的生理异常。肠菌产物胞壁酰二肽(MDP)是精神分裂症患者免疫激活的上游介质之一。Nod2作为一种细胞内的模式识别受体,可以特异性识别MDP,启动信号级联,释放炎性介质,支持早期宿主防御和免疫调节。因此,Nod2受体被称为“肠道守门员”,是维持肠道菌群和宿主免疫反应平衡的关键分子。此外,Nod2在肠道和大脑中均有广泛表达,是肠-脑轴的关键调节因子,是深入理解距离大脑较远的肠道菌群如何发挥作用的重要突破口。
孕期母体免疫激活(MIA)会破坏母体与胎儿环境的微妙平衡,导致子代出现持续的免疫改变、神经发育障碍和行为异常,因此MIA被认为是精神分裂症的重要风险因素。然而,并非所有母体感染都会导致子代出现精神分裂症或相关疾病,“遗传缺陷”可能使个体对MIA更易感,进而导致子代出现更严重的精神分裂症相关表型。马现仓教授团队前期研究发现,Nod2在精神分裂症患者中出现反应性受损,然而其对精神分裂症的影响机制仍不清楚。据此,该团队构建了Nod2-/-小鼠并创新性地建立了Nod2缺失联合MIA的双打击模型,揭示了Nod2缺失以性别依赖性的方式加重MIA诱导的子代精神分裂样行为。
该研究发现,Nod2基因缺陷与孕期免疫激活的双重暴露可导致雄性子代出现精神分裂症样行为,并伴随脑发育异常、肠道屏障损伤及微生物群紊乱。宏基因组分析进一步证实,母体肠道菌群失调可通过垂直传播影响子代,从而增加子代神经发育障碍风险。机制研究表明,这一过程涉及肠道完整性破坏、肠道类器官形成能力受损、神经递质信号异常以及胎儿脑内基因表达谱的显著改变。
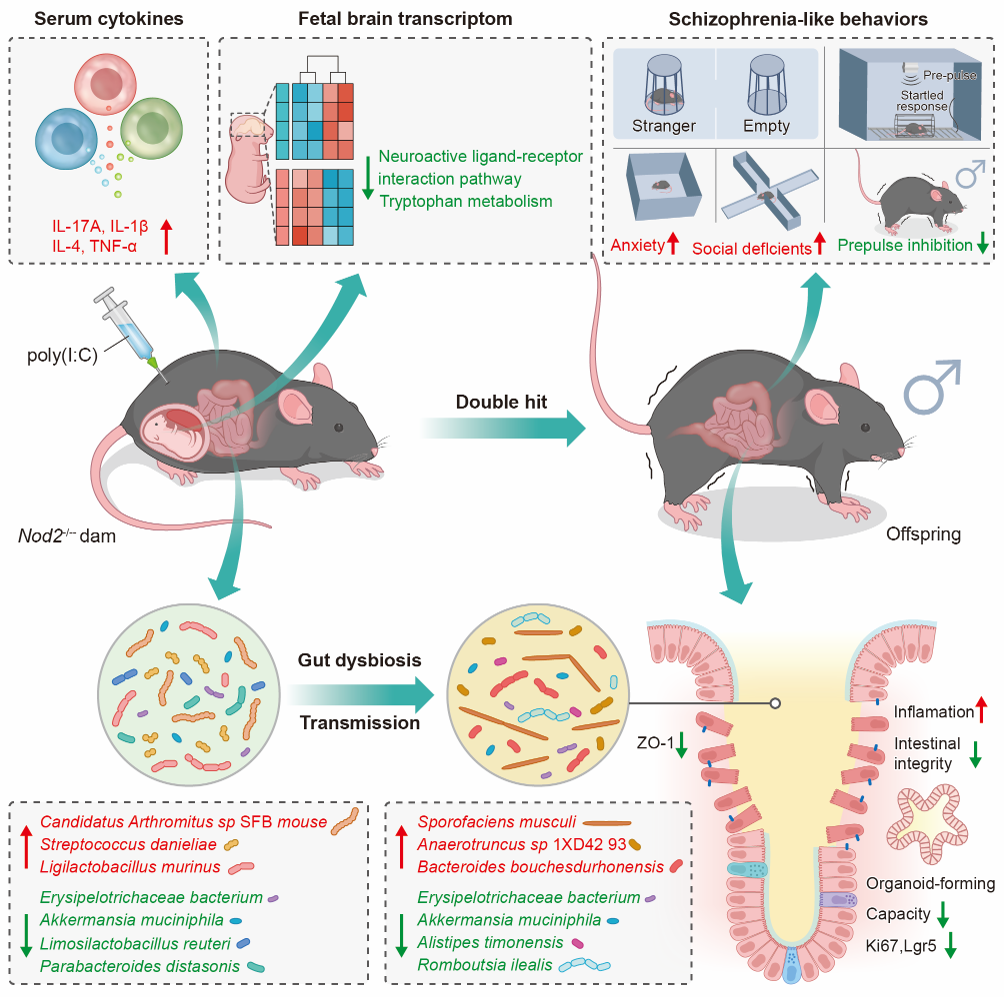
此项研究不仅为精神分裂症的“遗传-环境-微生物”交互作用理论提供了直接的实验证据,进一步证实了多因素共同作用在精神疾病发生发展中的重要性,同时也揭示了肠道微生物及其相关免疫通路在其中的关键角色。该成果为开发基于肠道免疫调控的精神疾病早期干预策略奠定了坚实的科学基础,开辟了通过调节肠道健康来改善精神健康的新视角。未来的研究可能聚焦于靶向Nod2通路调整特定菌群,这有望成为预防高危个体出现神经发育障碍的有效手段之一,为临床提供了一种新的个性化医疗思路。
本研究通讯作者为西安交大一附院精神心理卫生科马现仓教授和高媛博士后,第一作者为西安交大一附院精神心理卫生科高凤洁助理研究员和王楚瑶博士生,该成果是马现仓教授团队精神分裂症肠脑轴机制研究不断深入的结果。以上工作在陕西省生物精神病学重点实验室完成并获得国家自然科学基金、博士后基金等项目支持。

西安交通大学第一附属医院精神心理卫生科作为国内首批在综合医院开设医学心理门诊的学科,自1980年开设以来,便一直在精神心理卫生领域不断探索和创新。本研究团队围绕精神疾病的肠道菌群-免疫-脑轴机制不断深耕,并取得了一系列科研成果,先后在顶级期刊上发表多篇高水平学术论文,并促使了粪菌移植、益生菌干预等技术的临床转化与应用,形成了鲜明的学科特色,得到了国内外同行的高度评价和认可。
文章链接:https://www.sciencedirect.com/science/article/pii/S0889159125002077?via%3Dihub