近日,国际高水平学术期刊《细胞》出版社(Cell Press)公布了2024年“最受欢迎中国论文奖”,西安交大一附院袁祖贻、吴岳、李铤团队凭借其在《细胞-宿主与微生物》(Cell Host & Microbe)发表的论文《肠道菌群-胆汁酸通路维持被阿司匹林破坏的肠道稳态》(A gut microbiota-bile acid axis promotes intestinal homeostasis upon aspirin-mediated damage)在生命科学领域脱颖而出,获此殊荣。


团队代表李铤领奖
该成果发表于细胞杂志的微生物领域子刊《细胞-宿主与微生物》。论文系统阐明了阿司匹林引起肠道损伤的新机制,并首次提出通过“肠道菌群-胆汁酸轴”进行干预的策略,为阿司匹林等心血管药物副作用的防治提供了全新思路。阿司匹林作为全球最常用的药物之一,广泛应用于镇痛、抗血小板和肿瘤预防等领域。然而,其引发的胃肠道损伤问题长期困扰临床,超过90%的长期服药患者出现不同程度的肠道不良反应。尽管过去研究多关注于阿司匹林对前列腺素合成酶的抑制作用,但其引起肠道损伤的具体机制仍不明确。
本研究由西安交大一附院袁祖贻教授、吴岳教授、李铤教授以及美国国立医学院Frank J Gonzalez合作完成。团队通过整合分析临床队列多组学与动物实验结果,首次系统揭示了“肠道微生物-胆汁酸轴”在阿司匹林相关肠损伤中的关键保护作用。研究团队鉴定出一种受阿司匹林显著抑制的肠道共生菌——戈氏副拟杆菌(Parabacteroides goldsteinii),及其代谢产物7-酮石胆酸(7-keto-LCA)。后者在维持肠道稳态中发挥重要作用。实验表明,补充戈氏副拟杆菌能显著减轻阿司匹林引起的小鼠肠道屏障损伤。进一步机制研究揭示,7-keto-LCA作为法尼醇X受体(FXR)的拮抗剂,通过抑制FXR信号通路,激活Wnt信号,进而促进肠道干细胞的自我更新与上皮修复。该研究为阿司匹林相关肠病的防治提供了新的微生物—代谢干预思路:通过补充特定的益生菌(如戈氏副拟杆菌)或外源性胆汁酸代谢物,有望恢复肠道微生态平衡,减轻药物性肠损伤。

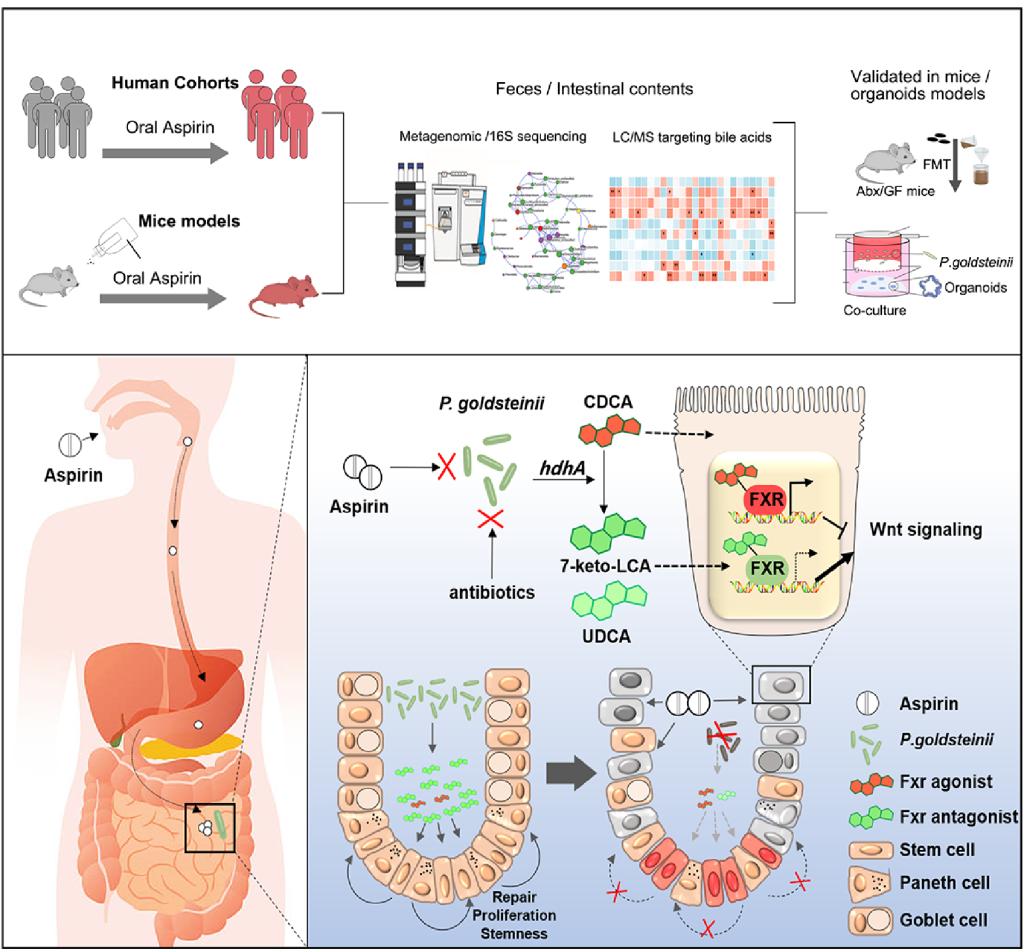
研究机制图
该项研究发表后受到国际同行高度关注,不但被《科学》等权威杂志发表论文引用,还在社交媒体、学术平台及公众科普领域引发讨论。研究成果不仅深化了对阿司匹林肠道副作用机制的理解,也为开发基于微生物组和代谢组的个体化胃肠道保护策略提供了重要理论依据。研究团队表示,未来将进一步开展临床转化研究,探索通过调节肠道菌群来预防和治疗阿司匹林相关肠道损伤的可行路径,推动“精准微生态治疗”在临床药学中的应用。论文链接:https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(23)00510-3
《细胞》出版社“中国年度论文奖”始于2014年,至今已连续举办十届。十年来,中国科学家在《细胞》出版社旗下期刊的发文量从初期逐年跃升,2024年达2446篇。本次奖项评选覆盖生命科学、物质科学、医学、交叉科学及可持续发展五大领域,经编辑部提名、第三方专家评审,并综合论文下载量、引用量、创新性等多重指标,最终评选出50篇“年度论文”及25篇“最受欢迎论文”。获奖论文代表了中国科研在各自领域的最高影响力与公众关注度。